みなさんこんにちは。
今回は簡易的な無機合成実験としてアルミホイルからミョウバンを合成したいと思います。ミョウバンくらい普通に買えやと思われるかもしれません。しかし、このような金属の単体から塩を合成することで学べることが多くあるのも事実です。早速、基礎知識について学んでいきましょう。
●アルミニウムについて
ミョウバンを合成するのに必要なのは第一にアルミニウムです。アルミニウムの歴史と性質について触れておきましょう。
【歴史】
アルミニウムは1825年に単体として分離されましたが、工業的に大量生産することが難しく、また、銀のように黒ずむことなくいつまでも輝かしい銀白色の光沢を保つことから「軽銀」と呼ばれて珍重され、一時は金よりも高価でした。しかし、1886年にアメリカの工学者ホールとフランスの工学者エルーが溶融電解法によるアルミニウム精製「ホール・エルー法」を発明しました。また、その後オーストリア=ハンガリー帝国の化学者バイヤーが発見したボーキサイトからアルミナを得る方法と共に今現在にまで受け継がれています。現在アルミニウムは軽量で加工が容易で安定、安価なことから1円硬貨やアルミ缶、アルミサッシ、アルミホイル、鍋、飛行機のボディ、各種合金など身近な場所で使われています。

アルミニウムの原料となるボーキサイト。土のような見た目をしている。
アルミニウムの製造においてアルミナ(酸化アルミニウム)は融点が2000度以上と高いので溶融するのは非常に困難です。そこで融点が1000度ほどの氷晶石(Na₃AlF₆)を溶融して溶媒とし、そこにアルミナを溶かし入れることで最終的に950度で電気分解を行えるようにしています。
電気分解では炭素電極を用い、各電極での反応式は、
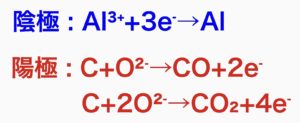
です。このように精製に電気分解を行うため電力消費が著しく、アルミニウムは別名電気の缶詰と呼ばれています。
【性質】
次にアルミニウムの性質について見てみましょう。アルミニウムは周期表の第13族に属する元素で銀白色の典型金属です。柔らかく、展性・延性に富み、熱や電気の伝導に優れています。単体は金や銀や銅とは異なり天然では産出しませんが、溶融電解法によって工業的に生産されています。
アルミニウムは価電子を3個持ち、3価の陽イオンになりやすいです。
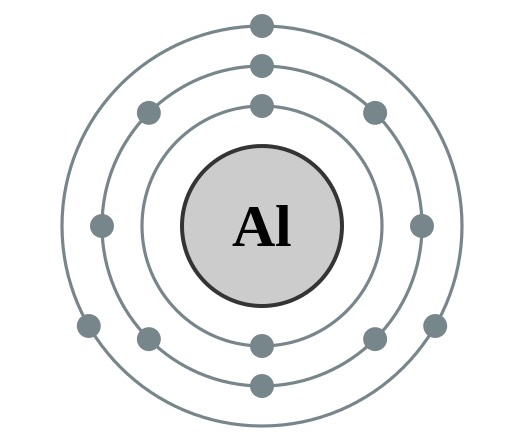
アルミニウムの表面は空気中で容易に酸化されますが緻密な酸化被膜を形成するため内部まで酸化が進行しません。
また、酸、塩基のどちらにも溶ける両性元素でもあります。

しかし、酸化力の強い濃硝酸などでは酸化被膜が生成し、不動態となるためそれ以上反応しません。

左:濃硝酸 右:濃塩酸
●塩について
化学的な塩についても話しておかなければなりません。塩は主に単塩、錯塩、複塩に分類されます。単塩という言葉自体はあまり使われることはないのですが複塩の対義語と思っていただければと思います。
・単塩
1種類の陽イオンと1種類の陰イオンからなる塩。塩化ナトリウムや水酸化カルシウム、硫酸ニッケルなど。
 |
 |
 |
| 塩化ナトリウム NaCl | 水酸化カルシウム Ca(OH)₂ | 硫酸ニッケル NiSO₄ |
・錯塩
塩を構成するイオンに錯イオン(金属イオンに非共有電子対をもつ陰イオンや分子が配位結合したイオン)が含まれるもの。ヘキサシアノ鉄(Ⅱ)酸カリウムやヘキサシアノ鉄(Ⅲ)酸カリウム、トリス(2,2\'-ビピリジル)ルテニウム(Ⅱ)ジクロリドなど。
 |
 |
 |
| ヘキサシアノ鉄(Ⅱ)酸カリウム | ヘキサシアノ鉄(Ⅲ)酸カリウム | トリス(2,2\'-ビピリジル) ルテニウム(Ⅱ)ジクロリド |
錯塩ではないですが、一応錯体の例としてヘキサクロロ白金酸も挙げておきます。
ヘキサクロロ白金(Ⅵ)酸
・複塩
構成する陽イオン、陰イオンが2種類以上であるもの。
酒石酸ナトリウムカリウム(ロッシェル塩)など。

酒石酸ナトリウムカリウム
今回合成するミョウバンは複塩にあたります。硫酸イオンなどの1種の陰イオンに対して三価と一価の2種の陽イオンで構成されているからです。
さて、基礎知識をそこそこに蓄えたところで今回どのようなプロトコルで合成実験を行なっていくか、化学反応式を交えて紹介したいと思います。
① 水酸化ナトリウムにアルミニウムを溶かす。
2Al+2NaOH+6H₂O→2Na[Al(OH)₄]+3H₂
② 未反応分をろ過し、ろ液に希硫酸を加える。
2Na[Al(OH)₄]+H₂SO₄→2Al(OH)₃+Na₂SO₄+2H₂O
③ ろ過で回収した水酸化アルミニウムに希硫酸を加えて完全に溶かす。
2Al(OH)₃+3H₂SO₄→Al₂(SO₄)₃+3H₂O
④ ③に硫酸カリウム水溶液を加える。
Al₂(SO₄)₃+K₂SO₄→2AlK(SO₄)₂
⑤ 加熱濃縮し、結晶を析出させる。
以上の手順で次回実際に結晶を作っていきましょう。
それではさよなラジカル。
えざお
〈実験編はこちら〉
≪≪ 戻る